-
Czym jest peeling enzymatyczny i jak go stosować?
Przeczytane 79113 razy
4 min
-
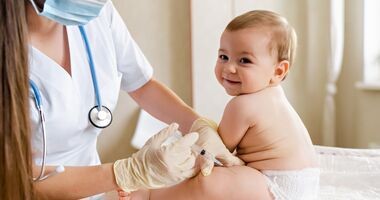
Szczepienia przeciwko meningokokom. Wskazania, liczba dawek szczepionek, skutki uboczne
Przeczytane 275866 razy
7 min
-
Grzybica pochwy – objawy i leki bez recepty. Kiedy i jak je stosować?
Przeczytane 396052 razy
5 min
-
Czym smarować nowy tatuaż? Jak dbać o skórę po zrobieniu tatuażu?
Przeczytane 77522 razy
5 min
-
Kawa a leki – interakcje, zagrożenia, zalecenia. Po jakim czasie od wzięcia leku można ją wypić?
Przeczytane 188 razy
5 min
-
Astma u dzieci – przyczyny, diagnostyka i objawy. Jak wygląda leczenie astmy oskrzelowej u dzieci?
Przeczytane 157 razy
7 min
-
Szczepienia dla podróżujących po Europie. Czy są obowiązkowe?
Przeczytane 868 razy
6 min
-
Antyperspirant a dezodorant. Jak je stosować, by skutecznie chronić się przed przykrym zapachem potu?
Przeczytane 69239 razy
6 min
-
Trądzik grzybiczy – przyczyny, objawy, leczenie, pielęgnacja
Przeczytane 449 razy
8 min
-
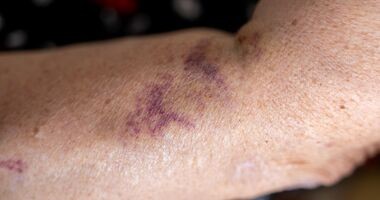
Wylewy podskórne u osób starszych. Przyczyny powstawania krwiaków podskórnych i wybroczyn
Przeczytane 358 razy
6 min


 Strefa okazji
Strefa okazji
 Nowości
Nowości
 Krótkie daty
Krótkie daty