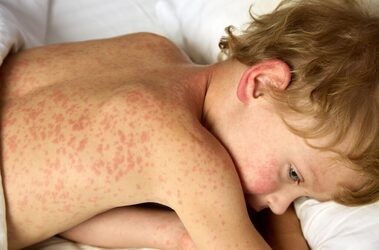
Terapia fagowa – wykazuje potencjał w leczeniu szigelozy
Wraz z rosnącą opornością bakterii na antybiotyki rośnie zainteresowanie alternatywami metodami leczenia, takimi jak terapia fagowa. Na czym ona polega? W jaki sposób może pomóc w leczeniu infekcji wywołanej przez bakterie z rodziny Shigella?
Zastosowanie terapii fagowej w leczeniu szigelozy
Wcześniejsze badania z wykorzystaniem bakterii Pseudomonas aeruginosa wykazały, że fagi i bakterie mogą angażować się w „ewolucyjne bitwy”, które powodują, że bakterie stają się bardziej wrażliwe na antybiotyki. Wyniki pracy opublikowanej w „Applied and Environmental Microbiology” sugerują, że trwający wśród drobnoustrojów wyścig zbrojeń może przyczynić się do powstania nowych sposobów leczenia zakażeń bakteryjnych, takich jak szigeloza.
Opracowanie antybiotyków, które będą w stanie zwalczyć nowo powstałe szczepy bakterii, jest pracochłonne i kosztowne. W związku z tym stale poszukiwane są alternatywne podejścia w leczeniu patogenów bakteryjnych. Jedną z możliwości jest terapia fagowa. Upatruje się ją jako potencjalną, tańszą opcję leczenia zakażeń wywołanych przez drobnoustroje oporne na antybiotyki. Bezpieczeństwo i wysoką skuteczność terapii tego rodzaju dokumentuje wiele prac naukowych.
Przeobrażając się, z czasem, bakterie mogą uodpornić się na bakteriofagi. Paul Turner, biolog ewolucyjny i wirusolog z Uniwersytetu Yale, stwierdził, że „bakterie są bardzo dobre w rozwijaniu odporności na fagi”, ale proces ten pociąga za sobą pewne konsekwencje. Bakterie nie przechodzą go bez szwanku.
Saima Aslam, lekarz chorób zakaźnych na Uniwersytecie Kalifornijskim w San Diego, niezaangażowana w ten projekt badawczy, wyjaśnia, że „nie zawsze jest źle”, gdy bakterie stają się odporne na fagi. Jeżeli w terapii zastosowano by odpowiedni rodzaj wirusa, mogłoby to ukierunkować ewolucję bakterii w taki sposób, aby były zdolne uciec przed drapieżnym bakteriofagiem, ale też jednocześnie stać się mniej zjadliwe. Mogłoby to wpłynąć na złagodzenie objawów infekcji.
Shigella flexneri — ewolucja patogenu przyczyniła się do zmniejszenia jego zjadliwości
Bakteria Shigella flexneri, która jest odpowiedzialna za wywołanie szigelozy, może unikać odporności gospodarza i rozprzestrzenianie się w wyściółce jelita powodować uszkodzenie tkanek. Zespół badaczy z Wydział Ekologii i Biologii Ewolucyjnej Uniwersytetu Yale w New Haven w Stanach Zjednoczonych stwierdził, że w warunkach laboratoryjnych gatunek ten ewoluował w kierunku pozwalającym uniknąć bakteriofaga, który je zabijał. Z powodu przemian bakterie stały się też mniej zjadliwe. Naukowców zastanawia, czy Shigella flexneri ewoluuje w ten sam sposób także poza naczyniem laboratoryjnym.
Naukowcy spostrzegli też zmiany w liposacharydzie — strukturalnym składniku komórek bakteryjnych. Jednym z wyjaśnień jest to, że te mutacje zniekształcają strukturę OmpA w taki sposób, że fag już jej nie rozpoznaje i nie może dostać się do komórek bakteryjnych. Kaitlyn E. Kortright, jedna z autorek badania, powiedziała, że mutacje w lipopolisacharydzie okazały się zaskoczeniem. Związek między tym składnikiem strukturalnym a OmpA nie został jeszcze w pełni wyjaśniony.



 Strefa okazji
Strefa okazji
 Nowości
Nowości
 Krótkie daty
Krótkie daty